Están bien mis modelos?
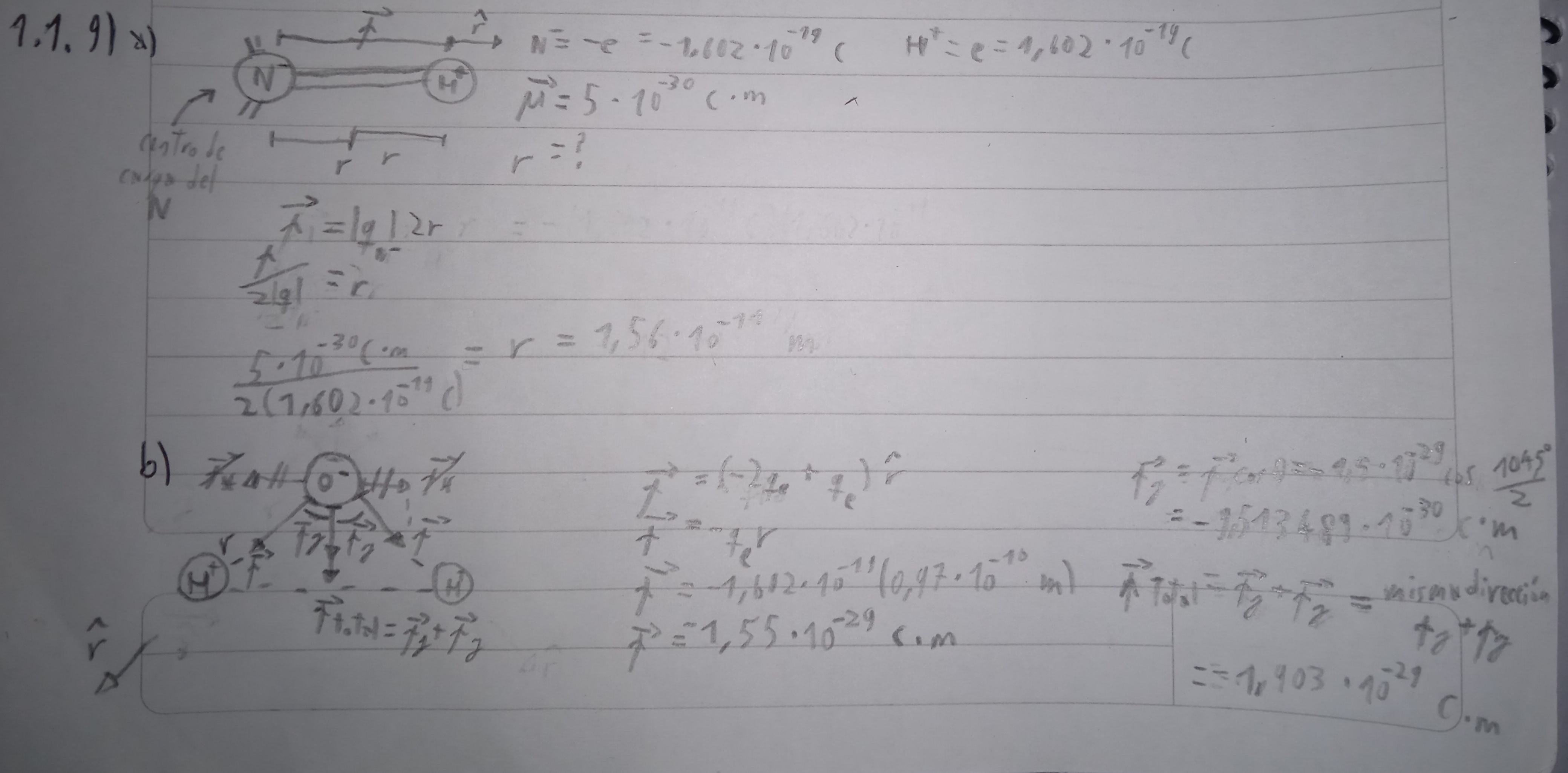 Además hay cosas que no había notado:
Además hay cosas que no había notado:
1) Qué carga uso en la ecuación del agua?
2) El vector momento dipolar no debería apuntar al átomo más electronegativo?
3) ¿"momento dipolar permanente" refiere al neto (molecular)?
Están bien mis modelos?
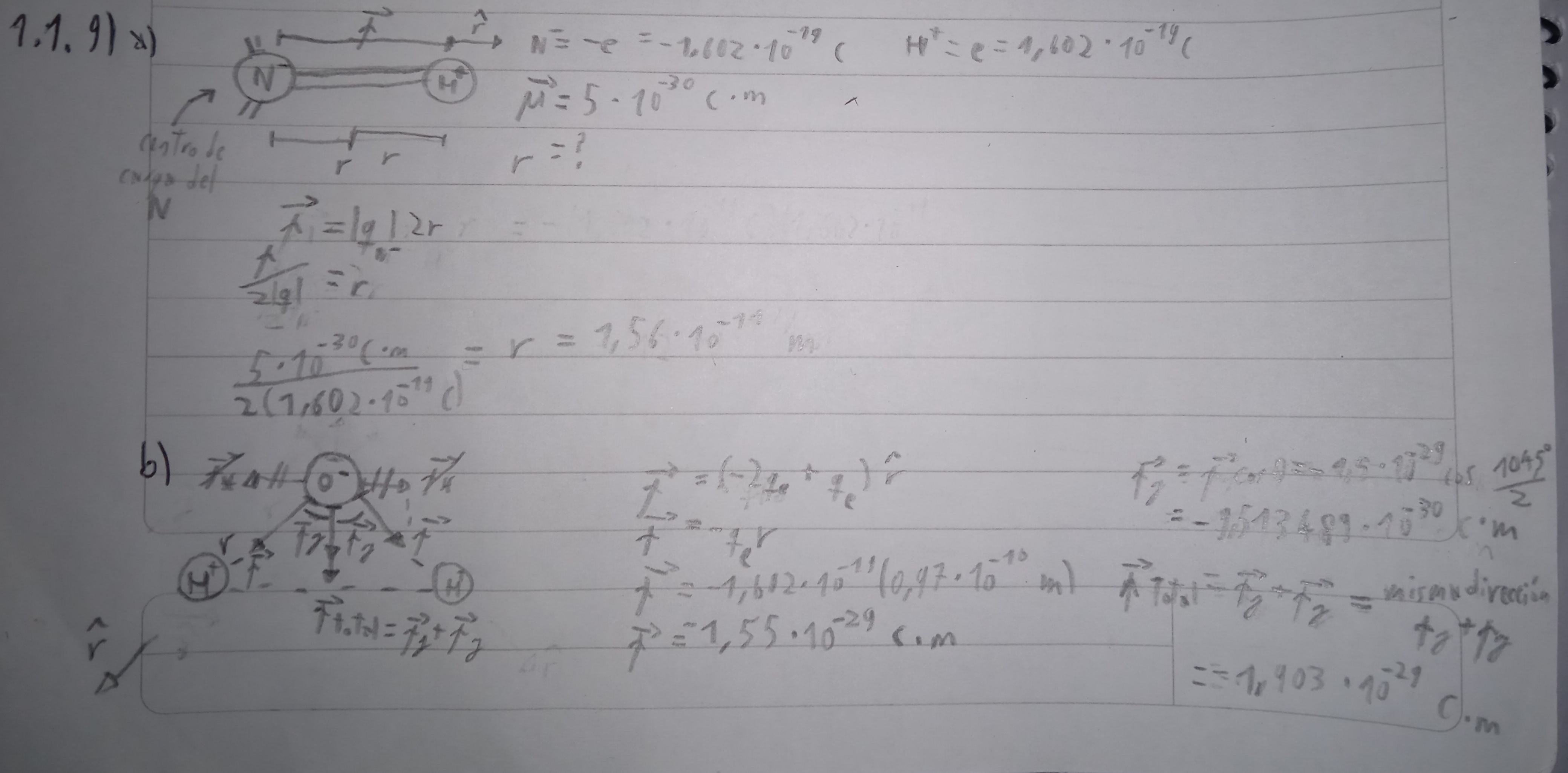 Además hay cosas que no había notado:
Además hay cosas que no había notado:
1) Qué carga uso en la ecuación del agua?
2) El vector momento dipolar no debería apuntar al átomo más electronegativo?
3) ¿"momento dipolar permanente" refiere al neto (molecular)?
Diego: la definición del momento dipolar (de su magnitud) es:
p= q.l = q.(2a)
Donde l, o 2a es la separación entre las cargas positivas y negativa o en general la distancia que hay entre el centro de carga positivo y el centro de carag negativo del dipolo.
En la parte a) calculas la mitad de la distancia.
Para la parte b) debes calcular p = q,l para el dipolo correspondiente a la molécula de agua. En este caso q es la magnituid de la carga ya sea positiva (la de los dos hidrógenos) o la negativa (la del oxígeno).
l (o 2a) es la separación entre los centros de carga. El centro de carga negativo coincide con el centro del átomo de oxígeni, mientras que el centro de carga positivo se encuentra en la mitad del segmento de recta que une los centros de los átomos de hidrógeno. En la figura que te adjunto, está marcado con una estrella.
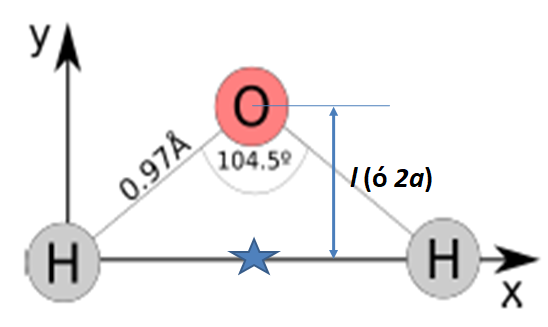
Con esta información, ¿te animás a recalcular el valor de p?